11. ऐल्कोहॉल, फिनाल एवं ईथर LONG ANSWER TYPE QUESTIONS
11. ऐल्कोहॉल, फिनाल एवं ईथर
प्रश्न 1. फीनॉल की अम्लता ऐल्कोहॉल की अपेक्षा अधिक है। क्यों ?
उत्तर⇒ फीनॉल की धातुओं (उदाहरणार्थ-सोडियम तथा ऐलुमिनियम) तथा सोडियम हाइड्रॉक्साइड के साथ अभिक्रियाएँ इसकी अम्लीय प्रकृति को दर्शाती है। फीनॉल में हाइड्रॉक्सिल समूह बेंजीन वलय के sp2 संकरित कार्बन से सीधा संयुक्त रहता है। जो कि इलेक्ट्रॉन अपनयक समूह के रूप में कार्य करता है।
किसी ऐल्कोहॉल तथा फिनॉल का आयनन निम्नलिखित प्रकार से होता है-

फीनॉल में – OH से संयुक्त sp2 संकरित कार्बन को उच्च विद्युत ऋणात्मकता के कारण ऑक्सीजन पर इलेक्ट्रॉन घनत्व कम हो जाता है। जिससे 0- H आबंध की ध्रुवता बढ़ती है।
ऐलकॉक्साइड आयनों ![]() में ऋणावेश ऑक्सीजन पर स्थानागत होता है। जबकि फीनॉक्साइड आयनों में विस्थापित होता है। ऋणावेश का विस्थानन संरचना (1 – V) फीनॉक्साइड आयनों को अधिक स्थायी बनाता है तथा फीनॉल के आयनन में सहायक होता है।
में ऋणावेश ऑक्सीजन पर स्थानागत होता है। जबकि फीनॉक्साइड आयनों में विस्थापित होता है। ऋणावेश का विस्थानन संरचना (1 – V) फीनॉक्साइड आयनों को अधिक स्थायी बनाता है तथा फीनॉल के आयनन में सहायक होता है।

प्रश्न 2. निम्नलिखित यौगिकों के IUPAC नाम लिखिए :


उत्तर⇒ (i) 2, 2, 4-ट्राईमिथाइल पेंटेन-3-ऑल
(ii) 5-इथाइल हेप्टेन-2, 4-डाइऑल
(iii) ब्यूटेन-2, 3-डाइऑल
(iv) प्रोपेन-1, 2, 3-ट्राइऑल
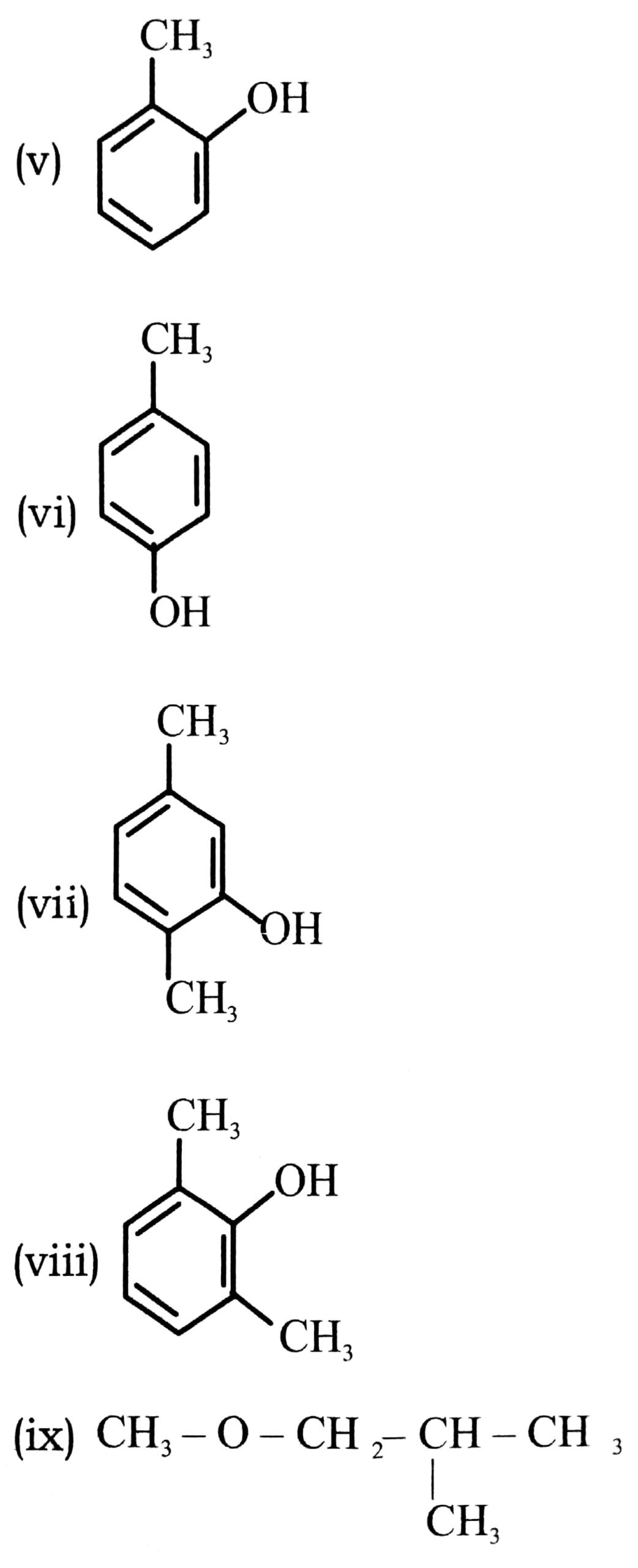
(v) 2-मेथिल फिनॉल
(vi) 4-मेथिल फिनॉल
(vii) 2, 5-डाइमेथिल फीनॉल
(viii) 2, 6-डाइमेथिल फीनॉल
(ix) 1-मिथॉलमा-2-मेथिलप्रोपेन
(x) एथॉक्सीबेंजीन
(xi) 1-फीनॉक्सीहेप्टेन
(xii) 2-एथॉक्सीब्यूटेन।
प्रश्न 3. निम्नलिखित अभिक्रियाओं के लिए समीकरण दीजिए।
(i) प्रोपेन-1-ऑल का क्षारीय KMnO4 के साथ ऑक्सीकरण।
(ii) ब्रोमीन की CS2 की फिनॉल से अभिक्रिया।
(iii) तनु HNO3 की फिनॉल से अभिक्रिया।
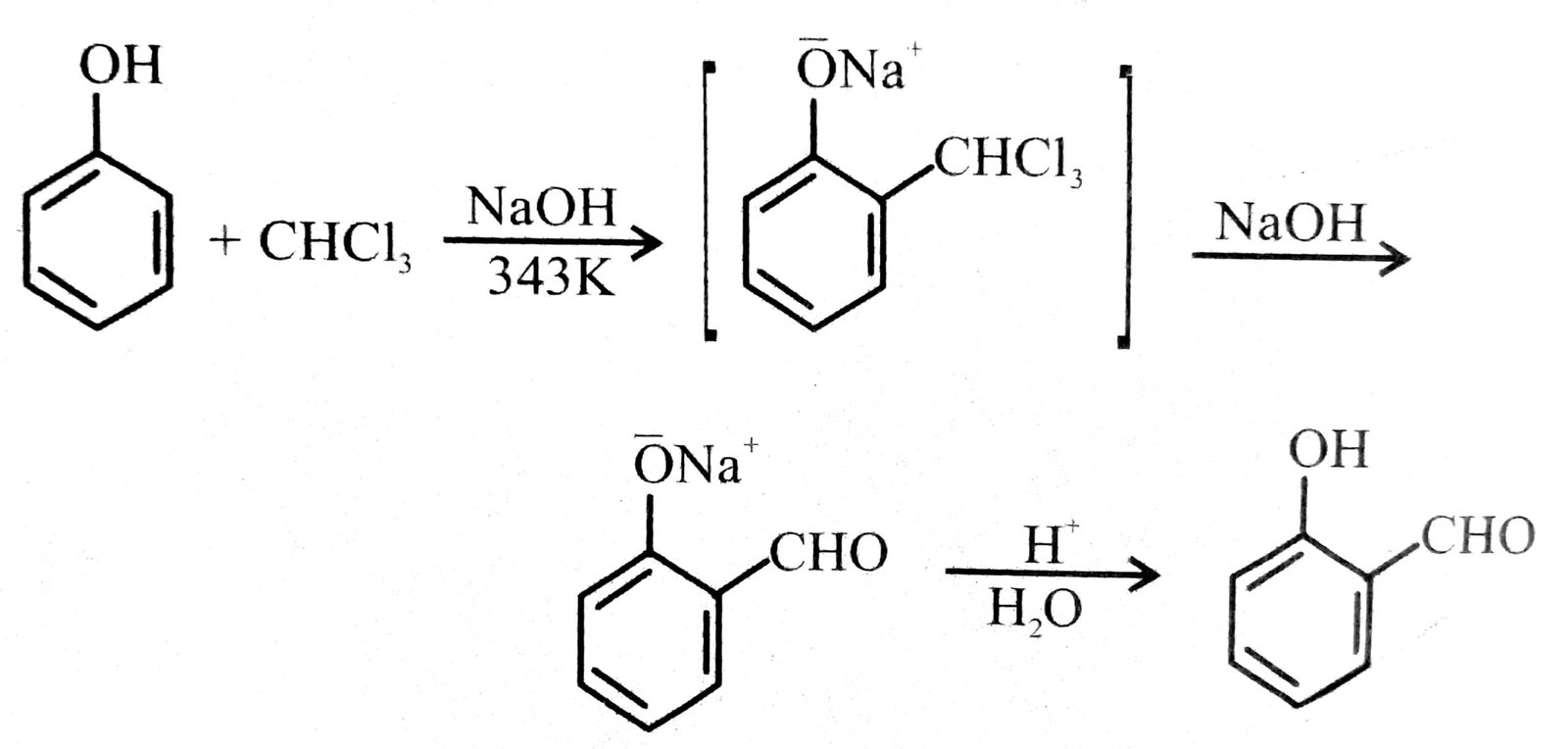
(iv) फिनॉल की जलीय NaOH की उपस्थिति में क्लोरोफॉर्म के साथ अभिक्रिया।
उत्तर⇒ (i) CH3CH2CH2OH + 2[O]![]() CH3CH2COOH + H2O
CH3CH2COOH + H2O
(ii) फिनॉल की ब्रोमीन व CS2 के साथ अभिक्रिया-

(iii) फिनॉल की तुन HNO3 के साथ अभिक्रिया

(iv) फिनॉल की CHCl3 व जलीय NaOH से अभिक्रिया
प्रश्न 4. निम्नलिखित को उदाहरण सहित समझाइए-
(i) विलियम्सन ईथर संश्लेषण
(ii) असममित ईथर।
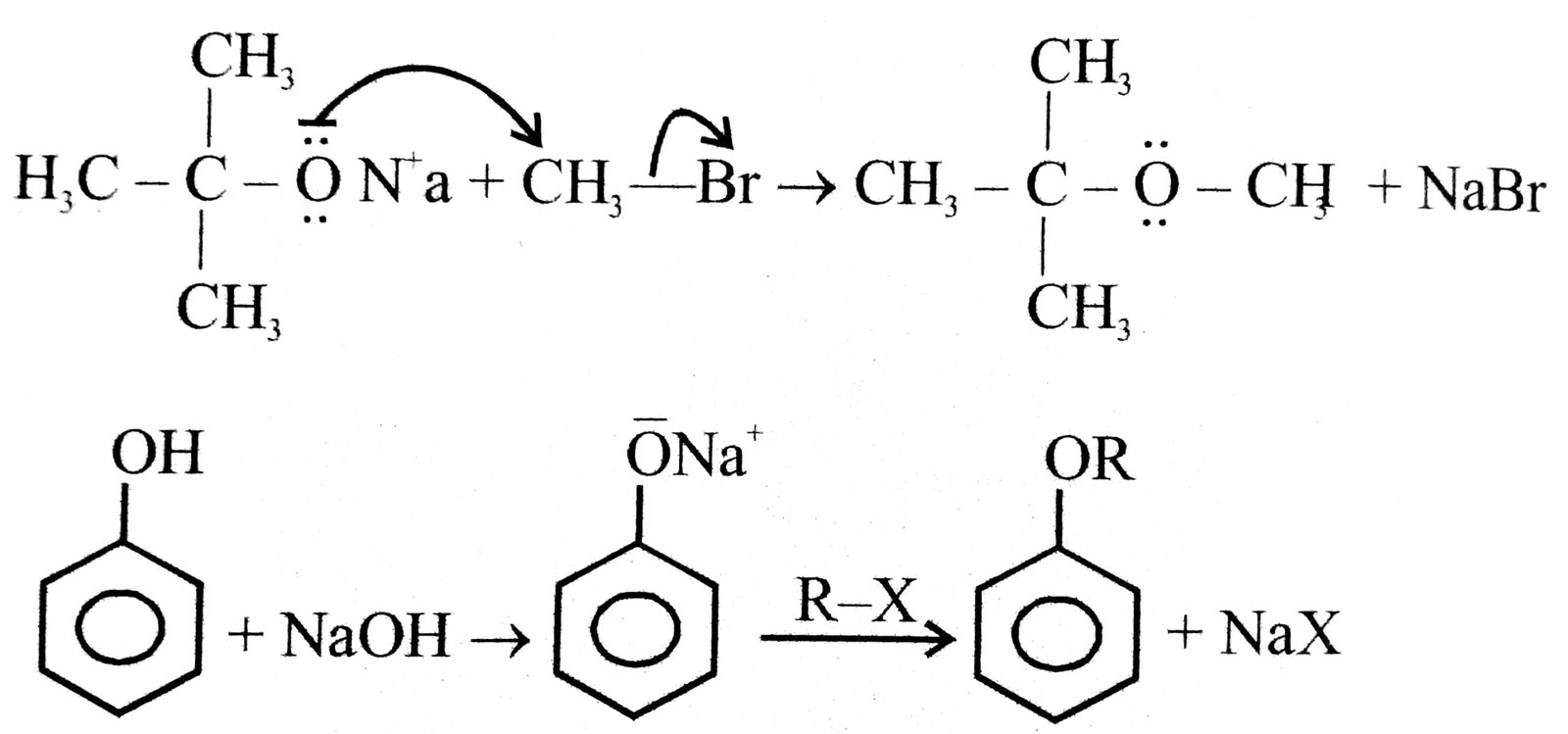
उत्तर⇒ (i) विलियम्सन ईथर संश्लेषण- यह सममित और असममित ईथरों को बनाने की एक महत्त्वपूर्ण प्रयोगशाला विधि है। इस विधि में, ऐल्क्लि हैलाइड की सोडियम ऐल्काक्साइड के साथ अभिक्रिया करायी जाती है।
R – C + R’ONa – R – O – R’ + NaX
इस अभिक्रिया में प्राथमिक ऐल्किल हैलाइड पर ऐल्काक्साइड आयन का SN2 आक्रमण होता है।
(ii) असममित ईथर- यदि ईथरल ऑक्सीजन के दोनों ओर दो विपरीत एल्काइल या ऐरिल समूह उपस्थित हो तो ऐसा ईथर असममित ईथर कहलाता है।
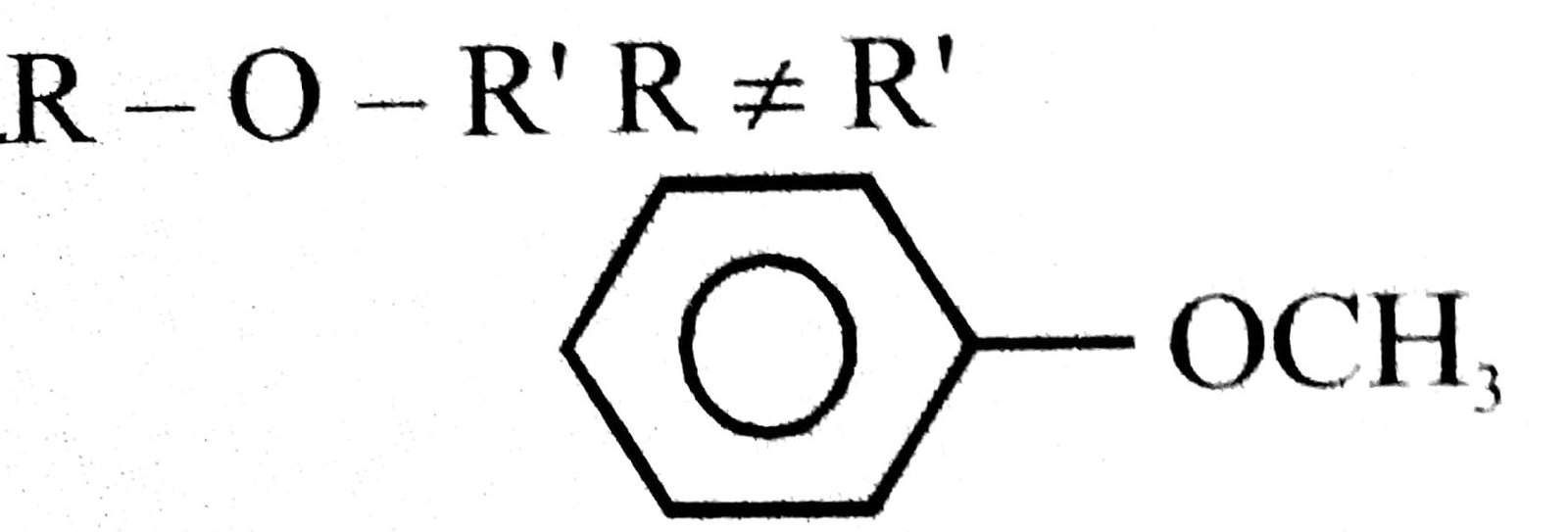
प्रश्न 5. हाइड्रोजन आयोडाइड की निम्नलिखित के साथ अभिक्रिया के लिए समीकरण लिखिए
(i) 1-प्रोपॉक्सीप्रोपेन (ii) मेथॉक्सीबेन्जीन तथा (iii) बेन्जिल एथिल ईथर
उत्तर⇒

प्रश्न 6. निम्नलिखित अभिक्रियाओं के लिए समीकरण लिखिए-
(i) फ्रिडेल-क्राफ्ट अभिक्रिया-ऐनिसोल का ऐल्किलन
(ii) ऐनिसोल का नाइट्रीकरण
(iii) एथेनॉइक अम्ल माध्यम में ऐनिसोल का ब्रोमीनन
(iv) ऐनिसोल का फ्रिडेल-क्राफ्ट ऐसीटिलन।
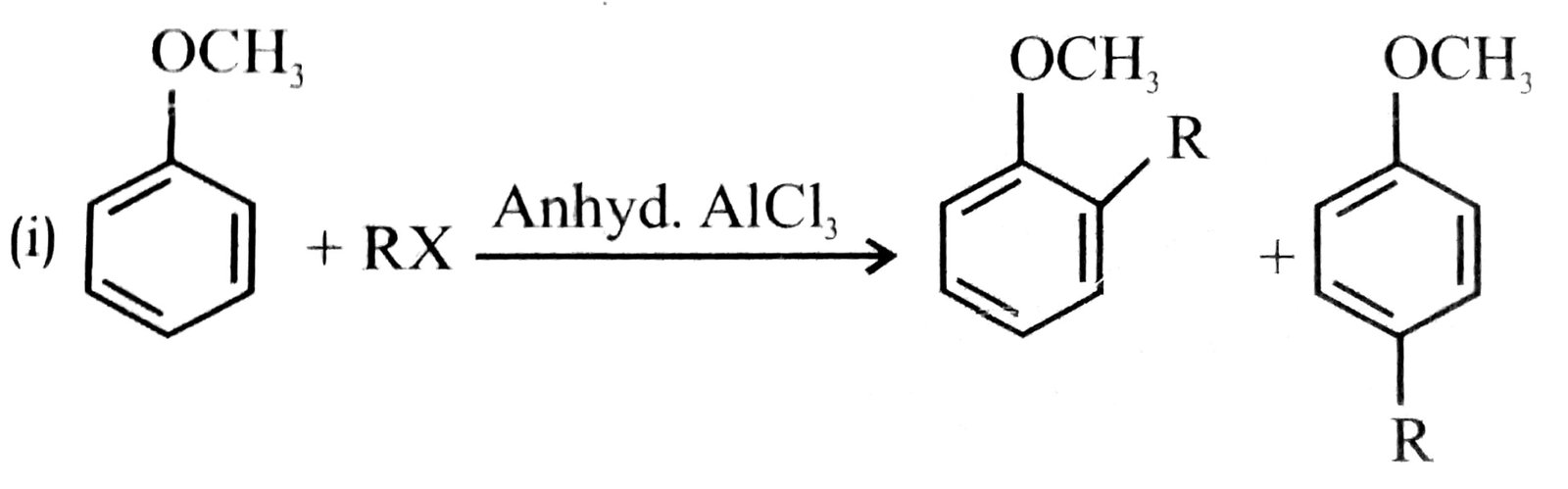
उत्तर⇒ (i) फ्रिडेल-क्राफ्ट अभिक्रिया-ऐनिसोल का ऐल्किलन-
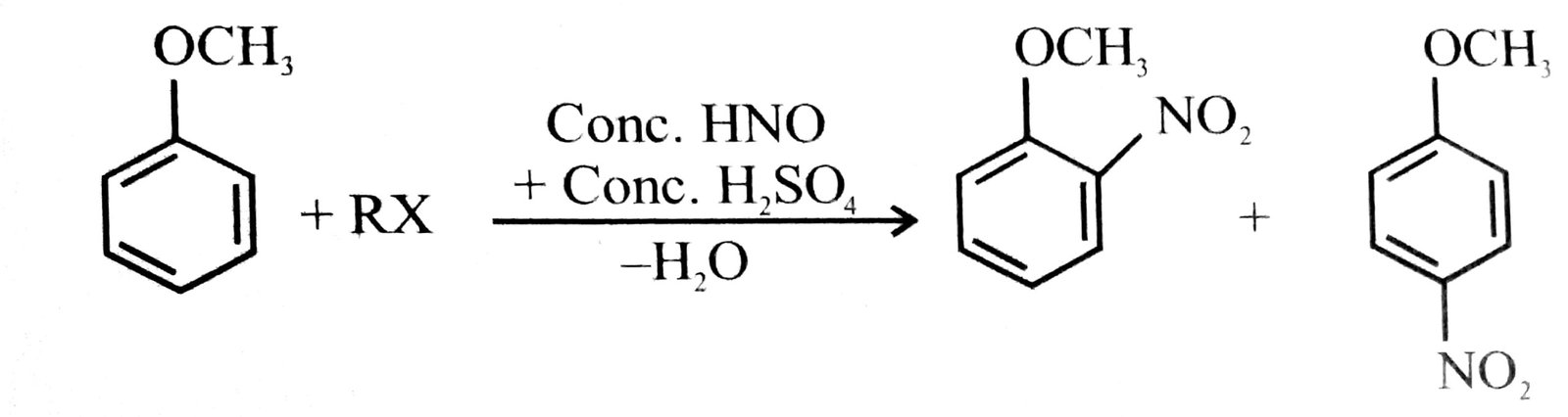
(ii) नाइट्रीकरण-एनिसोल जब सांद्र H2SO4 व HNO3 के मिश्रण से मिलता है तब आर्थों और पैरा नाइट्रो ऐनिसाल बनता है।
(iii) एथेनोइक अम्ल माध्यम में एनिसॉल का ब्रोमीकरण-फिनाइल एल्काइल इथर को हैलोजनन करते हैं जैसे एनिसॉल का ब्रोमीन कर ब्रोमो ऐनिसाल बनता है।

(iv) ऐनिसोल का फ्रिडेल-क्राफ्ट ऐसीटिलन-ऐनिसोल इलेक्ट्रॉन प्रतिस्थापन अभिक्रिया दर्शाता है तब इसे ऐसीटल क्लोराइड के साथ AICl3 की उपस्थिति में क्रियाशील किया जाता है। AlCl3 लेविस अम्ल की भाँति कार्य करता है। ऐसीटाइल वर्ग दोनों आर्थों और पैरा समूह पर आता है।

प्रश्न 7. मोनोहाइड्रिक ऐल्कोहॉल बनाने की विभिन्न सामान्य विधियों की विवेचना करें इनके सामान्य रासायनिक गुणों का वर्णन करें।
उत्तर⇒ मोनोहाइड्रिक ऐल्कोहॉल बनाने की सामान्य विधियाँ-
(i) ऐल्किल हैलाइड के जल-अपघटन (Hydrolysis) द्वारा-ऐल्किल हैलाइड का जलीय कास्टिल क्षार या आर्द्र सिल्वर ऑक्साइड द्वारा जल-अपघटन करने पर ऐल्कोहल प्राप्त होते हैं।
R-X + KOH→ RHO + KX
CH3I + KOH → CH3OH + CI
मिथिल आयोडाइड मेथिल ऐल्कोहॉल
R – CH2 – X + AgOH → R – CH2OH + AgX
CH3 – CH2 – Br→ CH3 – CH2OH + AgBr
एथिल ब्रोमाइड एथिल एल्कोहल
(i) ऐल्डिहाइड एवं कीटोन के अवकरण द्वारा- ऐल्डिहाइड एवं कीटोन का अवकरण करने पर एल्कोहल प्राप्त होता है। RCHO + 2[H] → R – CH2OH
. प्राथमिक ऐल्कोहॉल
R – CO – R’ + 2[H] → R – CH(OH) – R’
. द्वितीयक ऐल्कोहॉल
(iii) ग्रिगनार्ड-प्रतिकर्मक (Grignrd’s Reagent) द्वारा-ग्रिगनार्ड प्रतिकर्मक की प्रतिक्रिया फॉर्मल्डिहाइड, फॉर्मल्डिहाइड को छोड़ किसी दूसरे ऐल्डिहाइड तथा कीटोन से करने पर पहले योगशील यौगिक प्राप्त होते हैं।
इनका जल-अपघटन करने पर क्रमशः प्राथमिक, द्वितीय एवं तृतीय ऐल्कोहल प्राप्त होते हैं।

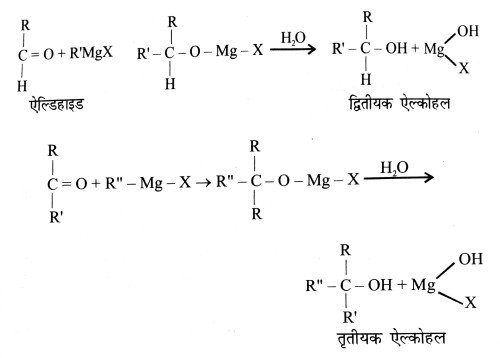
जहाँ R, R’ एवं R” तीन भिन्न ऐल्किल मूलक हैं।
ऐल्कोहल के सामान्य रासायनिक गुण-
1. ऑक्सीकरण (Oxidation)-
(क) प्राथमिक ऐल्कोहल को जलीय KMnO4 द्वारा ऑक्सीकृत करने पर कार्बोक्सिलिक अम्ल प्राप्त होते हैं।
R-CH2 – OH + 2[O]![]() R-COOH + H2O
R-COOH + H2O
प्राथमिक एल्कोहल कार्बोक्सिल अम्ल
CH3CH2CH2OH + 2[O]![]() CH3-CH2-COOH+H2O
CH3-CH2-COOH+H2O
प्रापिल एल्कोहल प्रोपायोनिक अम्ल
प्राथमिक ऐल्कोहॉल का ऑक्सीकरण पोटैशियम डाइक्रोमेट एवं सांद्र सल्फ्लूरिक अम्ल द्वारा कराने पर पहले ऐल्डिहाइड बनता है। जो पुनः ऑक्सीकृत होकर कार्बोक्सिलिक अम्ल में परिणत हो जाते हैं।
R -CH2OH+[O]![]() R – COOH + H2O
R – COOH + H2O
. कार्बोक्सिलिक अम्ल
CH3 -CH2 2OH + [O] ![]()
.CH3CH2CHO ![]() CH3CH2COOH
CH3CH2COOH
प्रोपायोनल्डिहाइड प्रोपायोनिक अम्ल
उपर्युक्त प्रतिक्रियाओं से स्पष्ट होता है कि प्राथमिक एल्कोहॉल के ऑक्सीकरण के फलस्वरूप प्राप्त ऐल्डिहाइड एवं अम्ल में कार्बन परमाणुओं की संख्या समान होती है।
(ख) द्वितीयक ऐल्कोहॉल का ऑक्सीकरण-द्वितीयक ऐल्कोहॉल का ऑक्सीकरण जलीय KMnO4 या K2Cr2O7 एवं सान्द्र H2SO4 द्वारा कराने पर ऐल्कोहॉल के समान कार्बन परमाणुओं की संख्या वाला कीटोन बनता है।
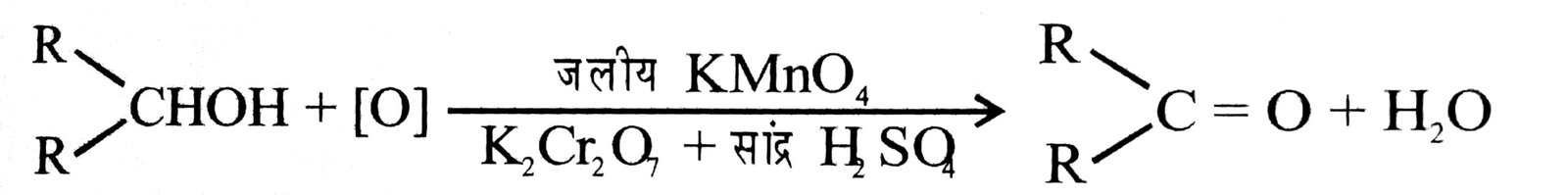
कीटोन एल्डिहाइड की तरह सुगमतापूर्वक ऑक्सीकृत नहीं होता है। यह प्रतिक्रिया की प्रचंड अवस्था में ऑक्सीकृत होकर ऐल्कोहॉल से एक कम कार्बन परमाणुओं की संख्या वाले कार्बोक्सिलिक अम्ल में परिणत हो जाते हैं।

(ग) तृतीयक ऐल्कोहॉल का ऑक्सीकरण-तृतीयक ऐल्कोहॉल उदासीन या क्षारीय घोल में ऑक्सीकरण का प्रतिरोधी होता है। किन्तु यह पोटैशियम डाइक्रोमेट एवं सांद्र सल्फ्यूरिक अम्ल द्वारा ऑक्सीकृत होकर पहले कीटोन तथा फिर अम्ल बनाता है।
इस प्रकार, तृतीयक ऐल्कोहॉल का ऑक्सीकरण होने पर कार्बन परमाणुओं की संख्या पहले ही चरण में घट जाती है।

2. एस्टरीकरण (Esterification)-अम्लीय उत्प्रेरक (HCl, H2SO4 तथा लूइस अम्ल BF3 आदि) की उपस्थिति में ऐल्कोहल कार्बोक्सिलिक अम्लों से प्रतिक्रिया कर एस्टर बनाते हैं।
R – COOH + H – O – R’![]() RCOOR’ + H2O
RCOOR’ + H2O
अम्ल ऐल्कोहॉल एस्टर
CH3COOH + HOC2H5 ![]() CH2COOC2H5 + H2O
CH2COOC2H5 + H2O
ऐसीटिक अम्ल ऐथिल एल्कोहॉल एथिल ऐसीटेट
ऐल्कोहल एवं अम्ल की प्रतिक्रिया द्वारा एस्टर बनने की क्रिया एस्टरीकरण कहलाती है।
3. सल्फ्यूरिक अम्ल की प्रतिक्रिया- अन्य अम्ल की तरह सल्फ्यूरिक अम्ल भी ऐल्कोहॉल से कमरे के ताप पर प्रतिक्रिया कर एस्टर बनाता है।
R – OH + HOSO3H → ROSO3H + H2O
. ऐल्किल हाइड्रोजन सल्फेट
सल्फ्यूरिक अम्ल द्वारा ऐल्कोहॉल जल निकलने की क्रिया निर्जलीकरण (dehydration) कहलाते हैं।
प्रश्न 8. ईथर बनाने की विभिन्न सामान्य विधियों की विवेचना करें। इनके सामान्य रासायनिक गुणों का वर्णन करें।
उत्तर⇒ ईथर बनाने की सामान्य विधियाँ-
(i) अल्काइल हैलाइड से-अल्काइल हैलाइड को सोडियम एल्कोसाइड के साथ गर्म करने से ईथर बनता है।
R – ONa + R – X → R – O – R + NaX
सोडियम अल्काइल ईथर
एल्कोसाइड हैलाइड
इसे विलियम्सन की विधि (Williamsons’ synthesis) कहते हैं।
C2H5 – ONa + C2H5I→ C2H5– O – C2H5+ NaI
सोडियम इथाइल डाइइथाइल ईथर
इथॉक्साइड आयोडाइड
(ii) अल्कोहल से- अल्कोहल के अधिक मात्रा को 140°C तक सान्द्र गन्धकाम्ल के साथ गर्म करने पर ईथर बनता है।
R – OH + R – OR![]() R – O – R + H2O
R – O – R + H2O
. ईथर
C2H5 -OH+H -O- C2H5![]() C2H5 -O-C2H5 +H2O
C2H5 -O-C2H5 +H2O
इथानॉल डाइइथाइल ईथर
(iii) अल्कोहल के निर्जलीकरण से-एल्कोहल को वाष्प के 250°C तक तप्त किए हुए एल्युमिनियम ऑक्साइड उत्प्रेरक के ऊपर प्रवाहित करने से जल का एक अणु निष्कासित होता है और ईथर बनता है।
R – OH + HOR![]() R – O – R + H2O
R – O – R + H2O
. ईथर
C2H5 – OH+HO – C2H5 ![]() C2H5 -O- C2H5 + H2O
C2H5 -O- C2H5 + H2O
. डाइइथाइल ईथर
ईथर का सामान्य रासायनिक गुण-
(i) HX के साथ प्रतिक्रिया-
R – O – R + HX![]() R – OH + RX
R – OH + RX
ईथर अल्कोहल अल्काइड
. हैलाइड
C2H5 – O – C2H5 + HI ![]() C2H5OH + C2H5I
C2H5OH + C2H5I
डाइ इथाइल ईथर इथाइल इथाइल
. अल्कोहल आयोडाइड
(ii) FCl5 के साथ प्रतिक्रिया- ईथर PCl5 के साथ प्रतिक्रिया कर अल्काइन क्लोराइड देता है।
R – O + PCl5![]() 2R – Cl + POCl3
2R – Cl + POCl3
ईथर अल्काइल क्लोराइड
C2H5 – O – C2H5 + PCl5 → 2C2H5Cl + POCl3
डाइ ईथाइल ईथर अल्काइल क्लोराइड
(iii) एसिड हैलाइड के साथ प्रतिक्रिया-ईथर, एसिद्ध हैलाइड के साथ अनार्द्र जिंक क्लोराइड की उपस्थिति में प्रतिक्रिया कर एस्टर बनाता है।